Es gibt keine Website-Inhalte zu Ihrer Suchanfrage.
Website-Inhalte
Sie haben sich erfolgreich abgemeldet.
Noch nicht registriert?
Es gibt keine Website-Inhalte zu Ihrer Suchanfrage.
Website-Inhalte
Es gibt keine Produkte zu Ihrer Suchanfrage.
Produkte
Entfalten Sie neue Räume für Fusion
Inspiriert von der menschlichen Anatomie, unterstützt durch Wissenschaft – unsere Cages verbinden technologische Fortschritte mit klinischen Werten. Das Ergebnis ist ein großer Sprung bei der anterioren und posterioren Stabilisierung.
Structan®
Glauben Sie, dass es sich um ein normales Käfiggitter handelt? Lassen Sie sich von der Wissenschaft hinter Structan® beeindrucken. Jahrzehntelange Erfahrung in Kombination mit moderner Technologie haben zur Entstehung einer Struktur geführt, die auf verbesserte klinische Ergebnisse und fortschrittliche biomechanische Leistung ausgelegt ist.
Die Oberfläche wird vergrößert um
0
Zeiten, was mehr Möglichkeiten für Knocheneinwuchs bietet.
Stark und elastisch zugleich – Structan® ist
0%
näher am Elastizitätsmodul der Kortikalis (1–4) *
Posteriore Stabilisierung mit nur
0
modulare Wirbelsäulenplattform, die sich exakt an Ihre Bedürfnisse anpasst.
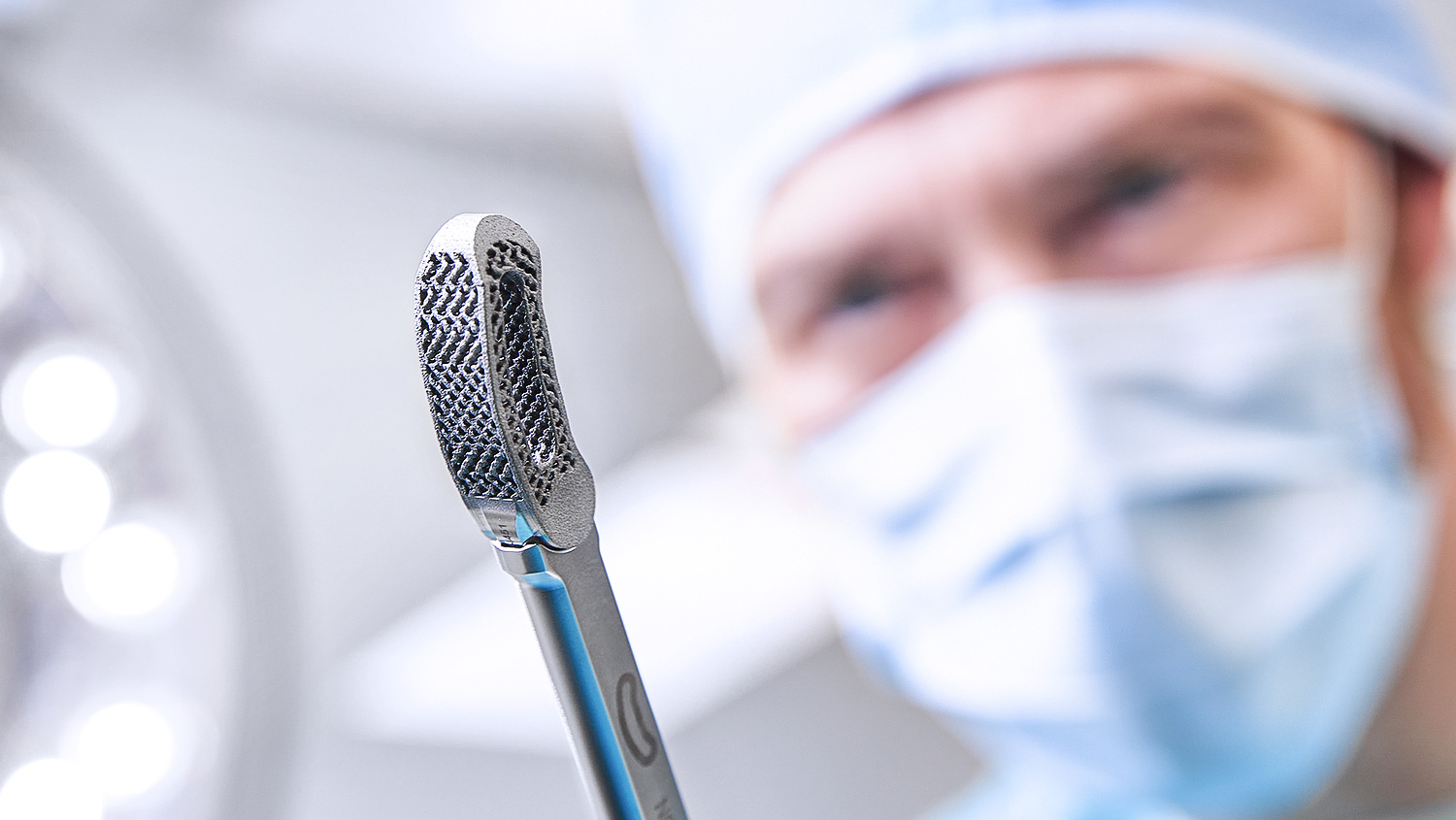
Die fein ausgewogene Oberflächenrauigkeit hat einen positiven Einfluss auf die Haftung von Osteoblasten. Die Porosität entspricht der menschlichen Anatomie. Dies schafft eine solide Basis für knöchernes Weiterwachsen und damit Fusion mit Structan®. [5–8]
/
Erhebliche osteoblastische Differenzierung und verbesserte Osseointegration – basierend auf wissenschaftlichen Erkenntnissen spiegeln unsere AESCULAP® 3D Cages die biologischen Attribute der trabekulären Struktur wider und fördern das knöcherne Einwachsen. [9–15]
/
Intelligent gestaltetes Transplantatfenster zur Unterstützung der Osseointegration zwischen Knochen und Implantat – mit oder ohne Autograft oder Allograft.
/
Die harmonisierte Schnittstelle bietet eine feste Verbindung zu den Instrumenten und eine hohe Präzision bei der Handhabung. Spüren Sie all dies mit unserem abwinkelbaren Inserter bei TLIF-Verfahren – denn Vertrauen gibt Sicherheit.
/
AESCULAP® 3D Wirbelkörperfusionsgeräte
Wie bei allen unseren Wirbelsäulenlösungen basiert auch das Design der AESCULAP® 3D Wirbelkörperfusionsimplantate auf unseren Kernwerten fortschrittliche biomechanische Leistung, intraoperative Flexibilität und verbesserte klinische Ergebnisse.
Additive Fertigung

Structan®
Produktpalette
Animationen zu chirurgischen Arbeitsabläufen
Sehen Sie sich die Leistungsfähigkeit der AESCULAP® 3D Wirbelkörperfusionsgeräte und Ennovate® an.
Unser TLIF Wirbelkörper-Versteifungsinstrument mit seinem abwinkelbaren Einführinstrument ermöglicht echte minimalinvasive Fusionsverfahren.
Mit ihrer optimierten Operationstechnik eignen sich unser PLIF Wirbelkörperfusionsgerät und Ennovate® ideal für den offenen Zugang.
Das Wesen zweier Welten verschmilzt – unser OLIF Wirbelkörperfusionsgerät kann sowohl minimalinvasiv als auch offen implantiert werden.
Entdecken Sie die AESCULAP® Wirbelsäulenplattform
*im Vergleich zu Implantaten für die Wirbelkörperfusion aus massiver Titanlegierung.
[1] Kuhn JL, Goldstein SA, Choi K, London M, Feldkamp LA, Matthews LS. Vergleich der trabekulären und kortikalen Gewebemoduli aus menschlichen Beckenkammbereichen. J Orthop Res. 1989;7(6):876 84.
[2] Ratner BD, Hoffmann AS, Schoen FJ, Lemons JE. Eine Einführung in Materialien in der Medizin. Akademischer Druck 1996.
[3] Chen Y, Wang X, Lu X, Yang L, Yang H, Yuan W, et al. Vergleich von Titan- und Polyetheretherketon (PEEK)-Cages bei der chirurgischen Behandlung einer mehrstufigen zervikalen spondylotischen Myelopathie: eine prospektive, randomisierte Kontrollstudie mit einer Nachbeobachtung über 7 Jahre. Eur Spine J. 2013;22(7):1539 46.
[4] Brizuela A et al. Einfluss des elastischen Moduls auf die Osseointegration von Zahnimplantaten. Materialien. 2019;12(6):980.
[5] Bostrom M, Boskey A, Kaufman J, Einhorn T. Form und Funktion des Knochens. Eingesetzt in: Orthopädische Grundlagenwissenschaft Biologie und Mechanik des Bewegungsapparats. 2. Ausgabe Rosemont, IL: AAOS; 2000: 320-369.
[6] Olivares-Navarrete R, Gittens RA, Schneider JM, et al. Raue Titanlegierungen regulieren die Osteoblastenproduktion angiogener Faktoren. Spine J 2012; 12:265-272.
[7] Lincks, J. et al. Die Reaktion von MG63-Osteoblast-ähnlichen Zellen auf Titan und Titanlegierungen hängt von der Oberflächenrauheit und -zusammensetzung ab. Biomaterialien 19, 1998. Seite 2219-32.
[8] Elias CN, et al. Mechanische und klinische Eigenschaften von Titan und Legierungen auf Titanbasis (Ti G2, Ti G4 kaltbearbeitet nanostrukturiert und Ti G5) für biomedizinische Anwendungen. Journal of Materials Research and Technology. 2019;8(1):1060 9.
[9] Cheng A, Cohen D, Boyan B et al. Lasergesinterte Konstruktionen mit bioinspirierter Porosität und Oberflächen-Mikro-/Nanorauigkeit verbessern die Differenzierung mesenchymaler Stammzellen und die Matrixmineralisierung in vitro. Calcif Tissue Int 2016; 99:625-637.
[10] Wu S-H, Li Y, Zang Y-Q, et al. Poröser Titan-6-Aluminium-4-Vanadium-Cage hat eine bessere Osseointegration und weniger Mikrobewegungen als ein Poly-Ether-Ether-Keton-Cage bei der Wirbelkörperfusion von Schafen. Kunstorgane 2013; 37:191–201
[11] Taniguchi N, Fujibayashi S, Takemoto M, Sasaki K, Otsuki B, Nakamura T, Matsushita T, Kokubo T, Matsuda S. Auswirkung der Porengröße auf das Einwachsen in poröse Titanimplantate aus additiver Fertigung: Ein in vivo Experiment. Werkstoffwissenschaft und -technik 2016; C59: 690–701.
[12] Changhui Song, Lisha Liu, Zhengtai Deng, Haoyang Lei, Fuzhen Yuan, Yongqiang Yang, Yueyue Li, Jiakuo Yu. Forschungsfortschritte bei der Entwicklung und Leistung von Knochenimplantaten aus poröser Titanlegierung. Journal of Materials Research and Technology, Band 23, 2023. Seiten 2626–2641, ISSN 2238-7854.
[13] Fukuda A, Takemoto M, Saito T, et al. Osteoinduktion von porösen Ti-Implantaten mit einer Kanalstruktur, die durch selektives Laserschmelzen hergestellt wird. Acta Biomat 2011; 7:2327-2336.
[14] Ran Q, Yang W, Hu Y, Shen X, Yu Y, Xiang Y, Cai K. Osteogenese von 3D-gedruckten porösen Ti6Al4V-Implantaten mit verschiedenen Porengrößen. J Mech Behav Biomed Mater. 2018 Aug;84:1-11. doi: 10,1016/j.jmbbm.2018.04.010. Epub 2018 18. April. PMID: 29709846.
[15] Van Bael S, Chai YC, Truscello S, Moesen M, Kerckhofs G, Van Oosterwyck H, Kruth JP, Schrooten J. Die Auswirkung der Porengeometrie auf das in vitro biologische Verhalten menschlicher periostal gewonnener Zellen, die auf selektiven lasergeschmolzenen Ti6Al4V-Knochengerüsten geimpft werden. Acta Biomater 2012 Jul;8(7):2824-34. doi: 10,1016/j.actbio.2012.04.001. Epub 2012 7. April. PMID: 22487930.
[16] Kia, C.; Antonacci, C.L.; Wellington, I.; Makanji, H.S.; Esmende, S.M. Osseointegration von Spinalimplantaten und die Rolle des 3D-Drucks: Eine Analyse und Überprüfung der Literatur. Bioengineering 2022, 9, 108. https://doi.org/10,3390/bioengineering9030108.
[17] Usability-Test, Usability Validation of AESCULAP® CeSPACE® 3D Cages, Tübingen, 2019.Die Usability des AESCULAP® 3D Cage-Systems CeSPACE® 3D wurde im April 2019 in einer Leichenwerkstatt mit sechs unabhängigen Testpersonen als vorgesehene Anwender (Chirurgen, die auf Wirbelsäulenchirurgie oder vergleichbare Bereiche spezialisiert sind) getestet. Unter anderem wurden Parameter wie die Sichtbarkeit des Implantats unter Röntgenkontrolle, die mechanische Stabilität der Implantat-Instrumenten-Schnittstelle und die Bewertung der Implantatoberfläche im Hinblick auf das Gewebeverletzungsrisiko getestet. Zu allen oben genannten Parametern wurden Akzeptanzkriterien erfüllt. Alle Testbenutzer bestätigten das Fehlen kritischer Merkmale, die vor der klinischen Anwendung verbessert werden müssen. Während des Tests wurde die Röntgensichtbarkeit der Cages besonders positiv bewertet.
[18] Rehnitz, Christoph, PD Dr. med. Röntgenbildauswertung von AESCULAP® Wirbelkörperfusionsgeräten, Heidelberg, 2019. CT- und Röntgen-Visualisierung verschiedener AESCULAP® Cages für die interkorporelle Fusion (vollständige Titan-, poröse Ti6Al4V- und PLASMAPOREXP®-Cages) wurden in einem Leichen-Setup getestet. Ein Radiologe beurteilte die Sichtbarkeit des Implantats und das Vorhandensein von Artefakten, die die Sicht auf benachbarte Strukturen einschränken könnten. Die Visualisierung und Beurteilung der Implantatposition wurde für alle getesteten Cages im Röntgenbild und CT durchgeführt. Kleinere Artefakte waren bei CT-Rekonstruktionen in der Umgebung von porösen Ti6Al4V- und Volltitanimplantaten sichtbar. Poröse Ti6Al4V-Implantate zeigten im CT im Vergleich zu Volltitanimplantaten etwas weniger Artefakte. Die beobachteten kleinen Artefakte schränkten die Beurteilung der umgebenden anatomischen Strukturen nicht ein.
With your personalized account, your online experience will be easier, more comfortable and safe.